骨科外固定支架产品注册技术审查指导原则
本指导原则旨在指导和规范骨科外固定支架产品的技术审评工作,帮助审评人员理解和掌握该类产品原理/机理、结构、性能、预期用途等内容,把握技术审评工作基本要求和尺度,对产品安全性、有效性作出系统评价。
本指导原则所确定的核心内容是在目前的科技认识水平和现有产品技术基础上形成的,因此,审评人员应注意其适宜性,密切关注适用标准及相关技术的最新进展,考虑产品的更新和变化。
本指导原则不作为法规强制执行,不包括行政审批要求。但是,审评人员需密切关注相关法规的变化,以确认申报产品是否符合法规要求。
一、适用范围
本指导原则适用于《医疗器械分类目录》中第二类骨科外固定支架(以下简称外固定支架),类代号现为6810。
二、技术审查要点
(一)产品名称的要求
外固定支架产品的命名应采用《医疗器械分类目录》或国家标准、行业标准上的通用名称,或以产品结构形式为依据命名,例如:单臂式外固定支架、环形外固定支架、组合式外固定支架等。
(二)产品的结构和组成
1. 产品的结构和组成
单臂式外固定支架可分为一体式和分体式两种类型,单臂一体式外固定支架主要由加压器、架体、万向球、夹针块、伸缩体等组成;单臂分体式外固定支架由直形杆(管)或异形杆(管)、可调节夹、万能关节等组成。
环形外固定支架主要由闭合环、开放环、环针夹、环杆(管)夹、直形杆(管)等组成。
组合式外固定支架一般是指由两套以上的单臂式和/或环形外固定支架组合在一起使用的产品,其结构组成应根据其具体的组合形式而确定。
2. 产品结构示意图
图1单臂一体式外固定支架
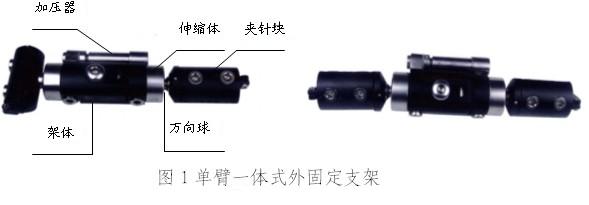
图2 单臂分体式外固定支架

图3 环形外固定支架
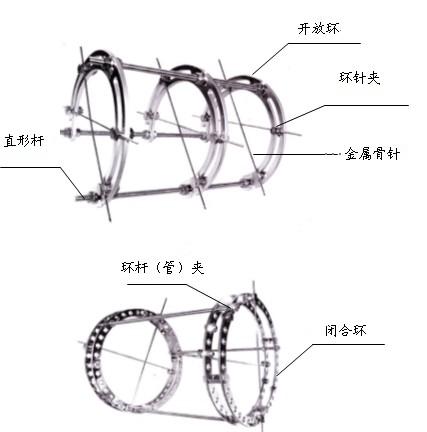
图4 组合式外固定支架

3. 产品材质
目前,骨科外固定支架大多采用铝合金、不锈钢、碳纤维棒和钛合金等四种材质制成。不锈钢应选用GB/T 1220-2007《不锈钢棒》中规定的20Cr13、30Cr13、40Cr13、95Cr18或更优质的原材料;铝合金应选用GB/T3190-1996《变形铝及铝合金化学成分》中所规定的2A12或更优质的原材料;钛合金材质应符合GB/T2965-2007《钛及钛合金棒材》的相关要求;选用碳纤维棒材质制成的部件,其力学性能中的抗弯强度和抗拉强度应不低于不锈钢材质制成的部件。
表1 骨科外固定支架各部件推荐材质表
|
部件名称 |
不锈钢 |
铝合金 |
碳纤维棒 |
钛合金 |
|
架体 |
|
√ |
√ |
|
|
夹针块 |
|
√ |
|
|
|
伸缩体 |
|
√ |
|
|
|
万向球 |
√ |
|
|
|
|
直形杆(管) |
√ |
|
√ |
√ |
|
异形杆(管) |
√ |
|
|
√ |
|
可调节夹 |
√ |
|
|
|
|
万能关节 |
√ |
|
|
|
|
闭合环 |
|
√ |
|
√ |
|
开放环 |
|
√ |
|
√ |
|
环针夹 |
√ |
|
|
|
|
环杆(管)夹 |
√ |
|
|
|
4.配套使用的器械
外固定支架可以配套使用的手术器械主要有快装手柄、钻头、导向器、保护套、钻套、上钉扳手、呆扳手、六方扳手等(属于第一类医疗器械)。可以与外固定支架配合使用的金属骨针为第三类医疗器械。
5.国内外产品情况
目前,国内外的外固定支架的产品结构、组成有所不同,一般国外产品包含配套使用的金属骨针,而国内的外固定支架和金属骨针因产品分类的不同,故多数制造商将外固定支架和金属骨针分别注册。其他配套使用器械基本相同,尺寸规格有所不同。
(三)产品工作原理
本产品工作原理与作用机理基本相同,在作用机理中描述。
(四)产品作用机理
骨科外固定支架是一种体外固定装置,它通过金属骨针将骨折各端与一个或多个的纵行杆(管)和/或环连接而达到稳定、复位的作用。
(五)产品适用的相关标准
1.相关的国家标准、行业标准
表2 相关产品标准
|
GB/T 230.1-2004 |
《金属洛氏硬度试验 第1部分 试验方法(A、B、C、D、E、F、G、H、K、N、T标尺)) |
|
GB/T 231.1-2002 |
《金属布氏硬度试验 第1部分 试验方法》 |
|
GB/T 1031-1995 |
《表面粗糙度 参数及其数值》 |
|
GB/T 1220-2007 |
《不锈钢棒》 |
|
GB/T 1804-2000 |
《一般公差 未注公差的线性和角度尺寸的公差》 |
|
GB/T 2965-2007 |
《钛及钛合金棒材》 |
|
GB/T 3190-1996 |
《变形铝及铝合金化学成分》 |
|
GB/T 4340.1-1999 |
《金属维氏硬度试验 第1部分 试验方法》 |
|
GB/T 8013.1-2007 |
《铝及铝合金阳极氧化膜与有机聚合膜 第一部份:阳极氧化膜 》 |
|
YY/T 0149-2006 |
《不锈钢医用器械 耐腐蚀性能试验方法》 |
上述标准包括了注册产品标准中经常涉及到的材质标准和性能标准。有的企业还会根据产品的特点引用一些行业外的标准和一些较为特殊的标准。
产品适用及引用标准的审查可以分两步来进行。首先对引用标准的齐全性和适宜性进行审查,也就是在编写注册产品标准时与产品相关的国家标准、行业标准是否进行了引用,以及引用是否准确。可以通过对注册产品标准中“规范性引用文件”是否引用了相关标准,以及所引用的标准是否适宜来进行审查。此时,应注意标准编号、标准名称是否完整规范,年代号是否有效。
其次对引用标准的采纳情况进行审查,即所引用的标准中的条款要求,是否在注册产品标准中进行了实质性的条款引用。这种引用通常采用两种方式,文字表述繁多内容复杂的可以直接引用标准及条文号。比较简单的也可以直接引述具体要求。
注意“规范性应用文件”和编制说明的区别,通常不宜直接引用或全面引用的标准不纳入规范性引用文件,而仅仅以参考文件在编制说明中出现。
如有新版强制性国家标准、行业标准发布实施,产品性能指标等要求应执行最新版本的国家标准、行业标准。
2.相关的国外标准
ASTM F 1541-02 《骨骼外部固定设备标准规范和检测方法》
(六)产品的预期用途
该产品通过与金属骨针的配合,应用于骨折部位的体外固定复位。
(七)产品的主要风险
外固定支架的风险管理报告应符合YY/T 0316-2003《医疗器械 风险管理对医疗器械的应用》的有关要求,审查要点包括:
1.产品定性定量分析是否准确(依据YY/T 0316-2003附录A审查);
2.危害分析是否全面(依据YY/T 0316-2003附录D审查);
3.风险可接收准则,降低风险的措施及采取措施后风险的可接收程度,是否有新的风险产生;
以下依据YY/T 0316-2003的附录D从两个方面提示性列举了外固定支架产品的危害因素及可采取的风险控制措施,提示审查人员从以下方面考虑:
表3 产品主要危害
|
可能的危害 |
危害的形成因素 |
可采取的风险控制措施 |
审查要点 |
|
A.功能性失效、维护不当引起的危害 |
|||
|
耐腐蚀性能 |
产品灭菌中受到腐蚀,使受腐蚀部分的力学性能降低。 |
选用合适的原材料制造外固定支架,耐腐蚀性不能满足要求的材料,应进行适当的表面处理,如:表面氧化或电镀等,以提高产品耐腐蚀性。 |
检查注册产品标准中是否对产品的耐腐蚀性能做出规定; 检查产品检测报告,对于耐腐蚀性能的检验是否合格; 检查产品使用说明书是否明确了产品的灭菌方法。 |
|
缺少维护规范和/或维护不适当 |
骨科外固定支架产品的维护保养应有适当的规范。如清洗规范、灭菌规范、搬运规范、贮存规范等,不然会造成维护不当,破坏骨科外固定支架的性能; 使用者未按规范进行适当的维护保养,破坏了骨科外固定支架的性能,如导杆变形、锁紧螺丝脱扣等,可能对患者产生影响达不到预期治疗效果的危害。 |
制定出完善的维护保养方法、运输、贮存要求和灭菌规则; 在随机文件中提示用户按照规定的维护保养方法和灭菌规则使用器械。
|
检查随机文件,其中应有维护保养方法、灭菌规则等内容; 检查注册产品标准中对产品包装是否提出要求; 检查风险管理文件的相关内容,应有防止维护不当危害的描述(包括该危害的风险分析、降低该风险的措施、可接受水平或剩余风险等内容)。
|
|
对外固定支架的使用期限缺少适当的规定 |
外固定支架在临床使用中有适当的使用期限,在使用期限外使用骨科外固定支架,会增大风险。
|
通过临床研究,给出外固定支架推荐的临床使用期限。
|
检查随机文件,其中应明确给出推荐的临床使用期限; 检查风险管理文件的相关内容,应有对缺少使用期限造成危害的分析(包括该危害的风险分析、降低该风险的措施、可接受水平或剩余风险等内容); 检查产品技术报告中对产品研制及临床情况的说明,是否可以证明产品临床使用期限的合理性。 |
|
B. 与外固定支架使用有关的危害 |
|||
|
不适当的操作说明 |
使用前检查规范不适当,如:未检查外固定支架的外观是否有裂纹,缺损、变形等缺陷;未检查产品各部件的配合是否良好; 外固定支架和/或与之配合的器械使用操作说明不适当,影响外固定支架的安装和稳定性,造成手术失败; 外固定支架的使用规范不适当,如灭菌方法不适当,导致性能降低、灭菌不彻底,对患者产生交叉感染等危害。 |
在产品使用说明书中明确产品使用前的检查规范和明确可与产品配合使用的器械。
|
检查风险管理文件的相关内容; 检查随机文件(使用说明书)中是否提示了使用前应检查外固定支架的外观、配合性能、包装是否破损、是否明确了产品配合使用的器械; 检查风险管理文件的相关内容,应有防止不适当操作说明危害的描述(包括该危害的风险分析、降低该风险的措施、可接受水平或剩余风险等内容)。
|
|
由不熟练/未经培训的人员使用 |
骨科外固定支架的安装应由经过培训的而且操作熟练的医生来完成,术后维护和紧固,应由经过培训的护理人员完成,否则可能造成骨折对位不良愈合或再移位。 |
编写产品使用手册,附赠视频操作光盘; 随机文件中应给出由经过培训操作熟练的医生使用的警示。 |
检查随机文件(使用说明书等),是否具有“必须由经必要培训而且操作熟练的医生使用”的内容和相关警示性说明。 检查风险管理文件的相关内容,应有防止由不熟练/未经培训的人员使用危害的描述(包括该危害的风险分析、降低该风险的措施、可接受水平或剩余风险等内容)。
|
|
对适应症和副作用的说明不充分 |
骨科外固定支架一般适用于闭合性和稳定性骨折,也适用于有广泛的软组织缺损的开放性骨折,不可用于严重的骨质疏松和伤肢有广泛的皮肤病患者,如对此说明不充分,可能会造成手术失败。 |
通过学术调查和临床研究,规范产品的预期用途和禁忌症; 依据临床调查研究结果,编写产品使用说明书中的预期用途和禁忌症。
|
检查随附文件中是否明确了产品的预期用途和禁忌症。 检查产品使用说明书中的预期用途和禁忌症是否与临床验证报告中的相关内容相吻合。
|
(八)产品的主要技术指标
本条款给出需要考虑的产品主要技术指标,其中部分技术指标给出定量要求,其他指标未给出定量要求,具体可参考相应的国家标准、行业标准。以下如有不适用条款(包括国家标准、行业标准要求),生产者应在产品标准的编制说明中说明理由。
1.产品材质:
参见第(二)条第3款的规定。
2.规格尺寸:
生产者应明确外固定支架的具体规格尺寸,尺寸大小及相应的公差要求,应参照有关的国家标准、行业标准或根据临床使用的要求制定。根据临床要求制定的规格尺寸,生产商应能够出示临床使用单位出具的证明性材料,证明性材料中应包含该外固定支架的适用人群及使用部位。
3.产品耐腐蚀性:
外固定支架中不锈钢部件的耐腐蚀性应能满足YY/T 0149-2006《不锈钢医用器械 耐腐蚀性能试验方法》中“沸水试验法”B级要求。
外固定支架中铝合金部件主要通过阳极氧化膜抵御外界腐蚀,故阳极氧化膜的性能决定了铝合金制件的耐腐蚀性能。铝合金制件的阳极氧化膜应符合国家标准GB/T 8013.1-2007《铝及铝合金阳极氧化膜与有机聚合膜 第一部份:阳极氧化膜》的规定。
碳纤维棒是由碳纤维丝拧合而成,暂不提出对耐腐蚀性能的要求。
4.整体配合性能:
在产品的研发阶段,建议参考ASTM F 1541-02《骨骼外部固定设备标准规范和检测方法》中模拟外固定支架配合金属骨针固定骨骼的试验,评价外固定支架和配套使用的金属骨针的整体配合性能。主要采用的试验方法有扭转试验、轴向加载试验、四点弯曲试验、悬臂弯曲试验。通过上述试验,绘制出应力-变形曲线,确定外固定支架及其配套使用的外固定针所构成的外固定系统在静态测量状态下的抗弯强度、弯曲屈服强度、最大弯曲力矩等,以及在动态测量状态下,产品的疲劳强度等性能指标。首次注册时,建议在产品技术报告中给出这些数值。
5.部件力学性能:
在产品的研发阶段,建议参照ASTM F 1541-02《骨骼外部固定设备标准规范和检测方法》中关于可调节夹、闭合环和开放环、直形杆(管)与可调节夹组成的局部组件的试验方法进行试验,绘制出应力-变形曲线并确定出上述各部件的刚度、屈服强度、极限强度等性能指标。首次注册时,建议在产品技术报告中给出这些数值,并在注册产品标准中给出重要的性能指标,如:刚度、强度等。
6.各部件的硬度:
根据所选用的不同材质和加工工艺,确定出不同部件的硬度,一般经热处理的部件硬度应不低于45HRC。
(九)产品的检测要求
产品的检测包括出厂检验和型式检验。
外固定支架产品的出厂检验项目一般应包括外观、尺寸、耐腐蚀性及硬度等;型式检验为产品标准全性能检验。
(十)产品的临床要求
1.首次上市的外固定支架产品应进行临床试用或临床验证,按照《医疗器械临床试验规定》的要求提交相关的临床试验资料。
如通过与同类已上市产品进行对比,可以论证该产品的技术性能指标优于同类已上市产品,则可申请豁免临床验证。
2.临床试验报告中应对外固定支架的适用范围、产品使用注意事项和产品的禁忌症等内容做出明确说明。
3.临床试验中主要观察项目:
耐疲劳性能;
抗弯曲能力;
整体配合稳定性。
4.外固定临床周期
临床观察周期要长于骨愈合期。
(十一)产品的不良事件历史记录
暂未见相关报道。
(十二)产品说明书、标签和包装标识
产品说明书、标签和包装标识的编写要求应符合《医疗器械说明书、标签和包装标识管理规定》和YY 0466-2003《医疗器械用于医疗器械标签、标记和提供信息的符号》的要求。
1.说明书内容:
(1)产品名称:
参见第(一)条“产品名称”的规定。
(2)商品名称:
如有商品名称,应符合有关产品商标管理的具体规定。名称应真实体现产品特点和企业特色,不得带有夸大产品宣传、误导使用的信息。
(3)注册证号:
核准的注册证号,如有变更情况的,应按变更后的注册证号编写。
(4)型号、规格:
产品型号中应体现出具体型号产品的临床应用部位,如:股骨单臂一体式外固定支架、指(趾)骨分体式外固定支架、胫骨环形外固定支架等。
按照注册证核准的型号、规格填写,不得擅自改变产品型号规格的文字表述。
(5)执行标准:
按照注册证标注的产品标准进行填写,并应标注标准年代号。
(6)主要结构及性能:
附产品结构示意图,具体将注册产品标准中所列重要信息予以注明,尤其是安全性、有效性性能指标和产品构成部件,如:产品所采用的原材料等。
(7)适用范围:
参见第(五)条“产品的预期用途”的规定。
(8)注意事项:
应明确配套使用的金属骨针;
建议产品一次性使用。
(9)禁忌症:
严重骨质疏松患者;
伤肢有广泛的皮肤病患者;
不能配合术后管理的患者。
(10)使用方法:
根据临床需要选择适宜规格的外固定支架;
选择与要使用的外固定支架相配套的金属骨针;
使用前应按照产品使用说明书中推荐的灭菌方法或选择符合要求的方法对产品进行灭菌;
将外固定支架与已固定在骨骼中的金属骨针进行连接,并且在必要时对骨折断端进行加压或撑开;
透视满意后将所有连接螺栓牢固锁紧;
按使用说明书规定的使用方法进行安装。
(11)运输、贮存方法:
外固定支架的运输和贮存方法应由制造者根据产品所用材质情况做出具体规定。一般应将外固定支架贮存在通风良好,无腐蚀性气体,相对湿度低于80%的室内。一般在运输过程中外固定支架产品应包装完好,具有防雨、防震措施。
2.标签和包装标识:
参照标准《医疗器械说明书、标签和包装标识管理规定》和YY/T 1052《手术器械标志》进行审查,说明书上应有相关标志的图示说明。
(十三)注册单元划分的原则和实例
外固定支架的注册单元的划分原则上以技术结构、性能指标和预期用途为划分依据。制造商应根据上述原则,按照自身产品特点划分注册单元。一般情况下单臂一体式外固定支架与其他形式的外固定支架应按照不同的注册单元划分。
(十四)同一注册单元中典型产品的确定原则
1.典型产品的确定原则
(1)典型产品应是同一注册单元内能够代表本单元内其他产品安全性和有效性的产品。应考虑功能最齐全、结构最复杂、风险最高的产品。
(2)注册单元内各种产品的主要性能不能被某一产品全部涵盖时,则应选择涵盖性能指标最多的产品作为典型产品,同时还应考虑其他产品中未被典型产品所涵盖的性能指标。
2.例如:注册单元中包含组合式外固定支架与单臂分体式外固定支架时,应选择组合式外固定支架作为典型产品。
骨科外固定支架产品注册技术审查指导原则编写说明
一、指导原则编写的原则
(一)本指导原则的编写目的是指导和规范第二类骨科外固定支架产品的技术审评工作。
(二)本指导原则旨在帮助审评人员理解和掌握该类产品原理/机理、结构、性能、预期用途等内容,把握技术审评工作基本要求和尺度,对产品安全性、有效性作出系统评价。
二、指导原则编写的依据
(一)《医疗器械监督管理条例》;
(二)《医疗器械注册管理办法》(局令第16号);
(三)《医疗器械临床试验规定》(局令第5号);
(四)《医疗器械说明书、标签和包装标识管理规定》(局令第10号);
(五)关于印发《境内第一类医疗器械注册审批操作规范(试行)》和《境内第二类医疗器械注册审批操作规范(试行)》的通知( 国食药监械[2005]73号);
(六)国家食品药品监督管理局发布的其他规范性文件。
三、指导原则中部分具体内容的编写考虑
(一)产品的结构和组成内容中,给出了骨科外固定支架典型产品的结构示意图,并简要介绍了骨科外固定支架的种类,同时对国内外产品发展情况进行了简单的比较。
(二)产品的作用机理中,介绍了骨科外固定支架的工作机理。本产品工作原理与作用机理基本相同,在作用机理中描述。
(三)列出了该类产品可参考引用的国外标准、国家标准和行业标准,参照相关的标准及法规要求,并综合考虑国外产品发展情况、产品特点和目前我国现有生产单位的技术条件,规定出了相应的技术指标。
(四)根据产品的临床应用情况,明确了产品的预期用途。
(五)产品的主要风险中,参照YY/T 0316-2003中附录D,逐项考虑骨科外固定支架可能产生的危害,以及降低风险的措施和技术审查时的要点。主要对产品的维护、保养,正确使用等方面的风险进行了详细的说明。
(六)在产品的检测要求中,引用了《医疗器械注册管理办法》第二章的规定,并对产品出厂检验的项目和要求做出了明确规定。
(七)针对骨科外固定支架产品特点,在使用说明书中对产品的性能、禁忌症、注意事项、使用、保养、维护、贮存等项目做出了规定。
(八)参照相关的法律、法规和临床使用要求,对骨科外固定支架的临床试验、临床验证以及豁免临床的条件做出了规定。同时对临床试验中重点观察项目做出了相应的说明。
四、其它产品
2002年版《医疗器械分类目录》外的其它第二类骨科外固定支架产品可参照本指导原则。
五、指导原则编写人员
本指导原则的编写成员由天津市食品药品监督管理局医疗器械产品注册技术审评人员、行政审批人员、国家食品药品监督管理局天津医疗器械质量监督检验中心专家、骨科外固定支架生产厂家代表、临床专家共同组成,充分收集各方面的信息和资源,综合考虑指导原则中各个方面的内容,尽量保证指导原则正确、全面、实用。